Энергетика группы атомов
*
Поговорим о том, что происходит, когда несколько атомов сближаются друг с другом. Для простоты ограничимся двумя атомами, для большего их числа все наши рассуждения и выводы останутся в силе. Не будем уточнять, образуется ли в результате сближения двух атомов молекула или какое-то другое их совместное состояние.
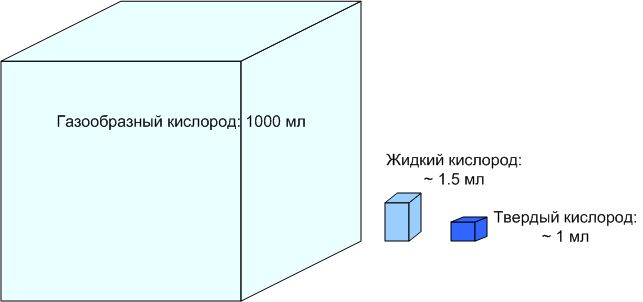
Давайте подумаем, почему существуют твердое и жидкое состояние? В принципе, частицы газа должны чувствовать себя наиболее комфортно - они свободны, их движение ничем не ограничивается. С точки зрения энтропии, состояние газа наиболее выгодно и желанно. Очевидно, переход в более конденсированные состояния (жидкость и газ) может регулироваться только принципом минимума энергии. Если общая энергия системы падает, у частиц газа просто недостает кинетической энергии, чтобы поддерживать скорость свободного полета. Именно поэтому при охлаждении газы сжижаются, а при дальнейшем охлаждении - затвердевают. Однако уменьшение скорости движения, по идее, не должно привести к уменьшению объема вещества. Если сильно охладить, скажем, один литр кислорода, который находился вначале при атмосферном давлении и температуре 25°С, то, исходя из одного только уменьшения скорости молекул, нужно было бы ожидать, что получится один литр жидкого кислорода. На практике получится чуть меньше полутора миллилитров (при температуре -183°С). А если продолжить охлаждение до затвердевания кислорода, то его окажется меньше миллилитра (при -252°С).
Получается, что вещество сильно сжимается, когда переходит в более конденсированное состояние. Особенно это заметно при переходе из газа в жидкость, хотя при затвердевании эффект сжатия тоже достаточен. Сжатие вещества означает, что расстояние между его частицами становятся меньше (поскольку число частиц не изменилось). Почему?
Очевидно, наиболее логичным будет предположение, что частицы вещества притягиваются друг к другу. Когда у частиц достаточно высокая кинетическая энергия (в газе), она позволяет им "не замечать" это притяжение. Однако когда кинетическая энергия становится меньше, именно притяжение между частицами заставляет их подойти ближе друг к другу. Природа притяжения частиц вещества друг к другу нас сейчас мало интересует. Скажем кратко, что дело тут во взаимодействии электронов и ядер соседних атомов друг с другом. Энергия притяжения атомов друг к другу описывается функцией вида E = Br-6, где r - расстояние между частицами, а B - некоторая постоянная, которая зависит от того, в каких единицах мы ведем расчет. Когда r велико, энергия притяжения пренебрежимо мала, частицы "не чувствуют" друг друга. Ecли же частицы в своих хаотических метаниях окажутся близко друг к другу, энергия притяжения может оказаться заметной. Если кинетическая энергия частиц будет высока (то есть если они движутся с высокой скоростью), они смогут вырваться из сил притяжения. Если же кинетическая энергия будет низкой, частицы начнут притягиваться все ближе и ближе, потому что чем ближе они притянутся друг к другу, тем более сильным станет притяжение.
Означает ли это, что атомы должны будут сблизиться бесконечно близко, то есть совпасть друг с другом? Ни в коем случае! При совпадении частиц друг с другом может произойти нарушение принципа Паули - некоторые электроны будут иметь полностью одинаковые характеристики, что недопустимо с точки зрения квантового мира. Поэтому при сближении атомов на "угрожающее" расстояние, начинают действовать силы отталкивания квантовой природы. Чем ближе будут подходить атомы, тем сильнее будет квантовое отталкивание. Энергия отталкивания описывается законом E = Ar-12, где r - расстояние между частицами, а A - некоторая постоянная (которая может быть равной B, а может отличаться от нее). Силы квантового отталкивания более мощные, чем силы притяжения, но они гораздо более короткодействующие, то есть они очень быстро убывают с увеличением расстояния между атомами.
Если теперь мы попробуем описать свободную энергию системы, состоящей из двух атомов, мы получим следующую картину:
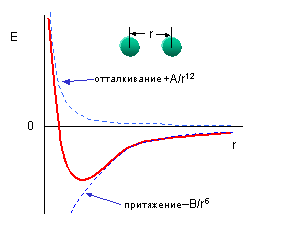 На большом удалении друг от друга свободная энергия системы будет равна нулю (будем считать, что кинетическая энергия движения атомов лежит вне нашего рассмотрения и считается поэтому связанной, то есть несвободной). При сближении атомов на некоторое достаточно большое расстояние (в правом конце нашего графика) начнут действовать силы притяжения. Притяжение скрепляет нашу систему, значит ее свободная энергия уменьшается. Процесс понижения свободной энергии системы продолжается, и постепенно атомы сближаются на такое расстояние, на котором становятся заметными силы квантового отталкивания. Силы отталкивания более мощные, поэтому очень скоро продолжение сближения начинает приводить не к уменьшению, а к резкому росту свободной энергии системы. Все это описывается уравнением Леннарда-Джонса:
На большом удалении друг от друга свободная энергия системы будет равна нулю (будем считать, что кинетическая энергия движения атомов лежит вне нашего рассмотрения и считается поэтому связанной, то есть несвободной). При сближении атомов на некоторое достаточно большое расстояние (в правом конце нашего графика) начнут действовать силы притяжения. Притяжение скрепляет нашу систему, значит ее свободная энергия уменьшается. Процесс понижения свободной энергии системы продолжается, и постепенно атомы сближаются на такое расстояние, на котором становятся заметными силы квантового отталкивания. Силы отталкивания более мощные, поэтому очень скоро продолжение сближения начинает приводить не к уменьшению, а к резкому росту свободной энергии системы. Все это описывается уравнением Леннарда-Джонса:
E = Ar-12 + Br-6
Самое важное в этой ситуации то, что уравнение Леннарда-Джонса (и его график на рисунке) показывают, что существует некоторое расстояние, на котором энергия системы будет минимальна. Это расстояние соответствует "потенциальной яме" - очень устойчивому состоянию, в котором наша система будет стремиться остаться на возможно большее время. Любое другое положение атомов друг по отношению к другу энергетически менее выгодно, чем нахождение их на расстоянии, соответствующем наиболее глубокой точке потенциальной ямы. Это расстояние принято называть равновесным расстоянием, а любое отклонение от него - нарушением равновесия, ведущим к росту свободной энергии.
- Subscribe
- Блог пользователя lugovsa
- Войдите, чтобы оставлять комментарии
Новые записи в блогах
- Как добиться популярности в TikTok
- Как производятся памятники из гранита
- Фильм «Джон Картер» - жизнь на Марсе есть
- Театр-Музей Сальвадора Дали и замок Пуболь
- Игровой автомат Golden Games в казино Эльдорадо
- SlotV с небывалой отдачей
- Шоп туры в Италию
- Пляжный отдых в Греции и Испании
- Заработок без вложений - как поднять денег на играх.
- ТОП достопримечательностей Берлина



Новые комментарии